
IKATAN KOVALEN TUNGGAL MOLEKUL H2O (AIR) YouTube
Pelarutan Senyawa Ionik dan Kovalen. Ngomong-ngomong tentang larutan, terbentuknya itu kan karena adanya interaksi antara zat terlarut dan zat pelarut. Nah, yang namanya interaksi, berarti kita akan nyerempet-nyerempet ke jenis ikatan kimia, seperti ikatan ionik, kovalen, polar, dan nonpolar. Contohnya larutan garam (NaCl) dilarutkan oleh air.

Ikatan Kovalen Adalah
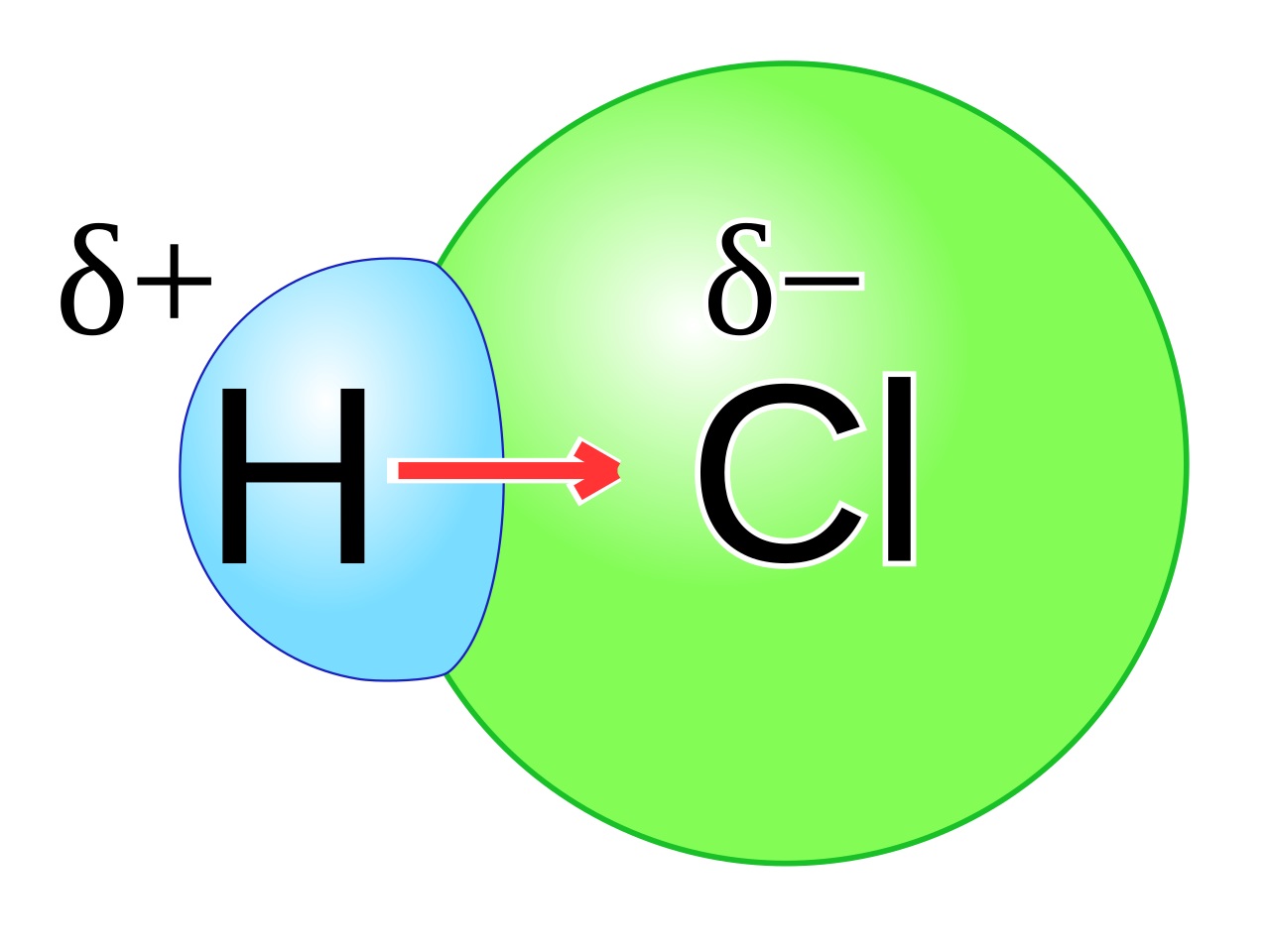
Ilustrasi ikatan kovalen polar seperti contoh berikut ini: Contoh ikatan kovalen polar.. Contoh senyawa lain yang memiliki bentuk molekul simetris dan bersifat nonpolar adalah CH 4, BH 3, BCl 3, PCl 5, dan CO 2. Perhatikan struktur salah satu ikatan kovalen non Polar dari CH 4 berikut:

🔴IKATAN KOVALEN POLAR & NON POLAR, 🔴SENYAWA KOVALEN POLAR DAN SENYAWA KOVALEN NONPOLAR YouTube
Beberapa contoh senyawa ikatan kovalen di antaranya adalah senyawa HCl, CH4, O2, N2, C2N2, CO, C3H4, dan HCN. 2. Ikatan Logam Ikatan logam adalah ikatan yang terjadi pada logam akibat tarik-menarik kation di dalam lautan elektron yang bertindak sebagai perekat dan menggabungkan kation-kation.
10 Contoh Ikatan Kovalen Polar dan Non Polar dalam Kehidupan Seharihari Materi Kimia
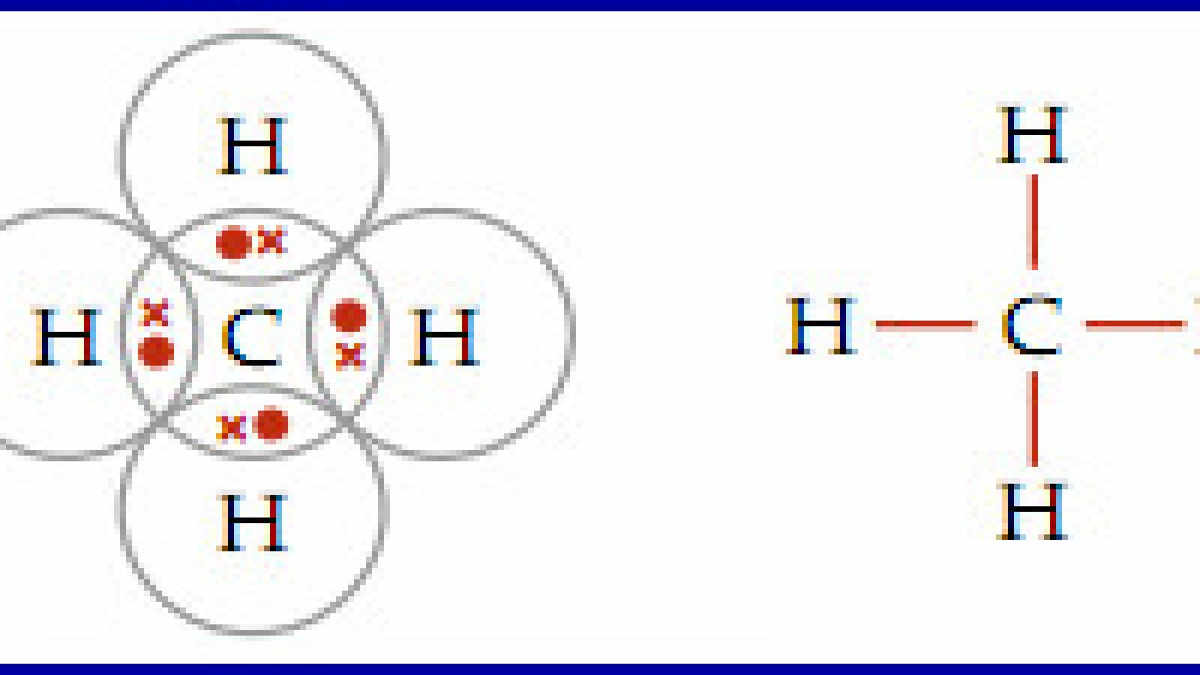
Nah, sekarang coba deh, perhatikan contoh pembentukan ikatan kovalen tunggal pada senyawa CH 4 berikut ini. Konfigurasi elektron atom 6 C: 2, 4. Jadi, atom C memiliki 4 elektron valensi, sedangkan atom H konfigurasinya hanya 1 saja, atau memiliki 1 elektron valensi.
Senyawa yang Memiliki Ikatan Kovalen Tunggal dan Koordinasi
50 Contoh Senyawa yang Memiliki Ikatan Kovalen Beserta Jenisnya - Dalam pelajaran kimia, kamu akan menemukan materi tentang ikatan kovalen. Merupakan ikatan yang terbentuk dari pemakaian bersama pasangan elektron antara dua atom, ikatan kovalen ini biasanya terjadi antara atom-atom non logam. Dalam artikel kali ini akan dibahas lebih jauh.
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
Contoh ikatan kovalen jenis ini adalah pembentukan senyawa HCl dan CH4. a. Pembentukan HCl. Konfigurasi elektron 1H : 1s1 sehingga elektron valensinya = 1. Untuk mencapai konfigurasi elektron yang stabil (sesuai kaidah duplet) diperlukan 1 elektron. Konfiguarsi elektron 17Cl adalah 1s2 2s2 2p6 3s2 3p5 sehingga CI dan mempunyai elektron valensi = 7.
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
Ikatan kovalen juga mencakup beberapa macam interaksi, seperti ikatan σ, ikatan π, ikatan logam-ke-logam, interaksi agostik, ikatan bengkok, ikatan tiga pusat dua elektron (3c-2e), dan tiga pusat empat. ikatan-elektron (3c-4e). Berikut adalah beberapa contoh ikatan kovalen dalam kehidupan sehari-hari.
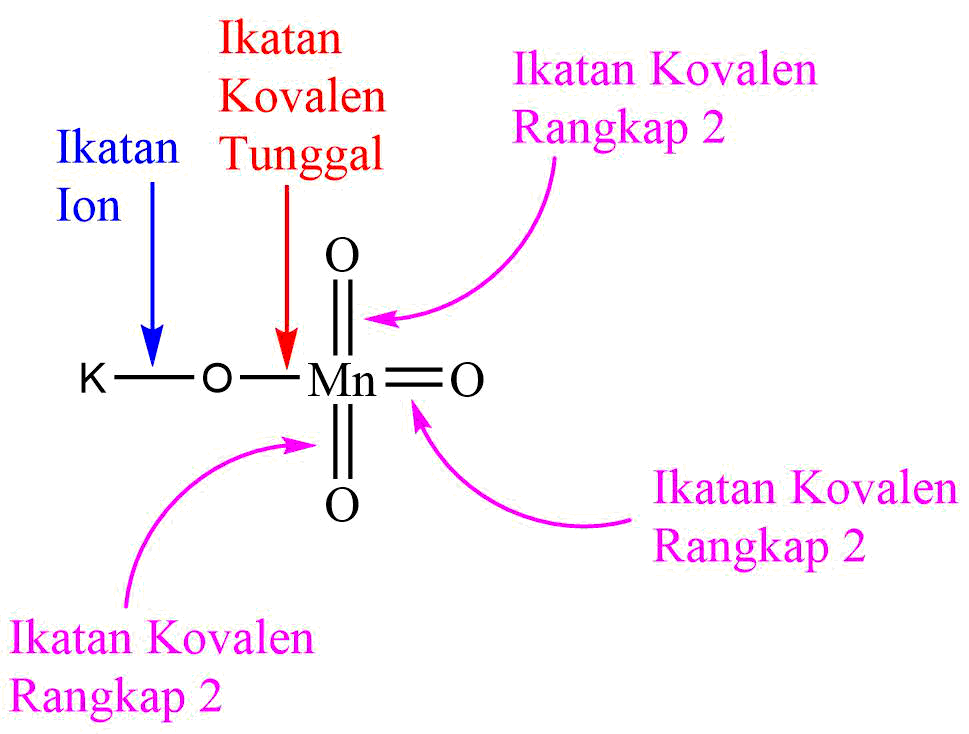
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
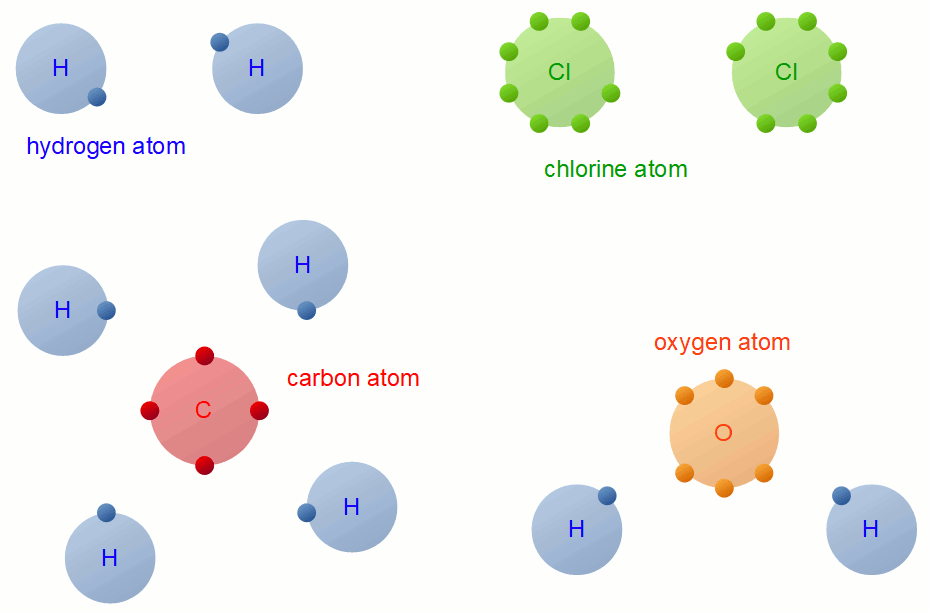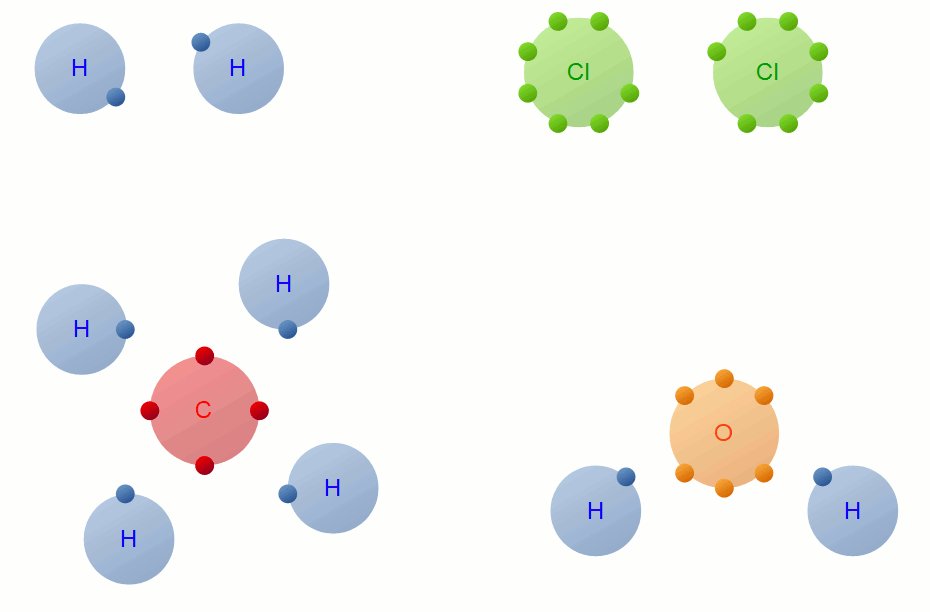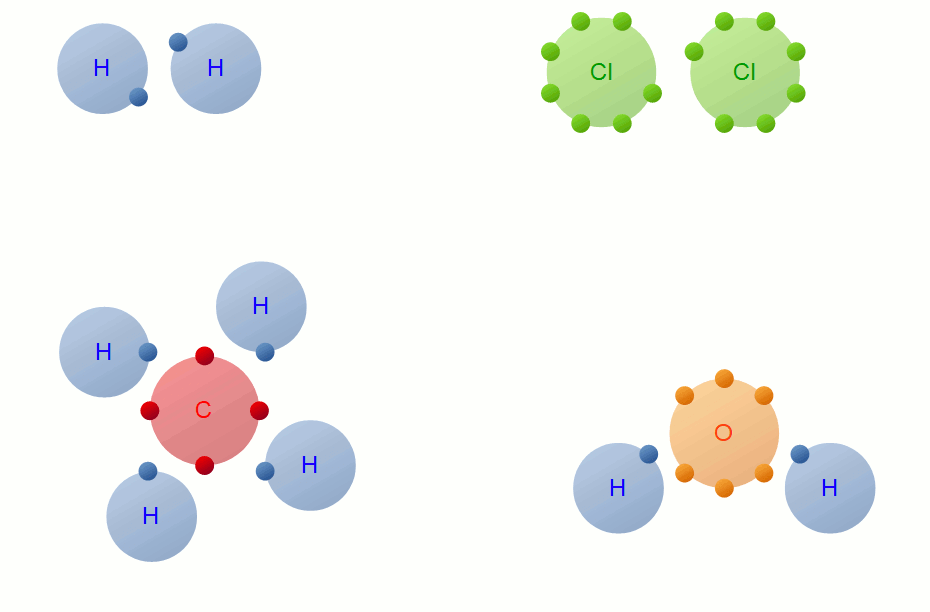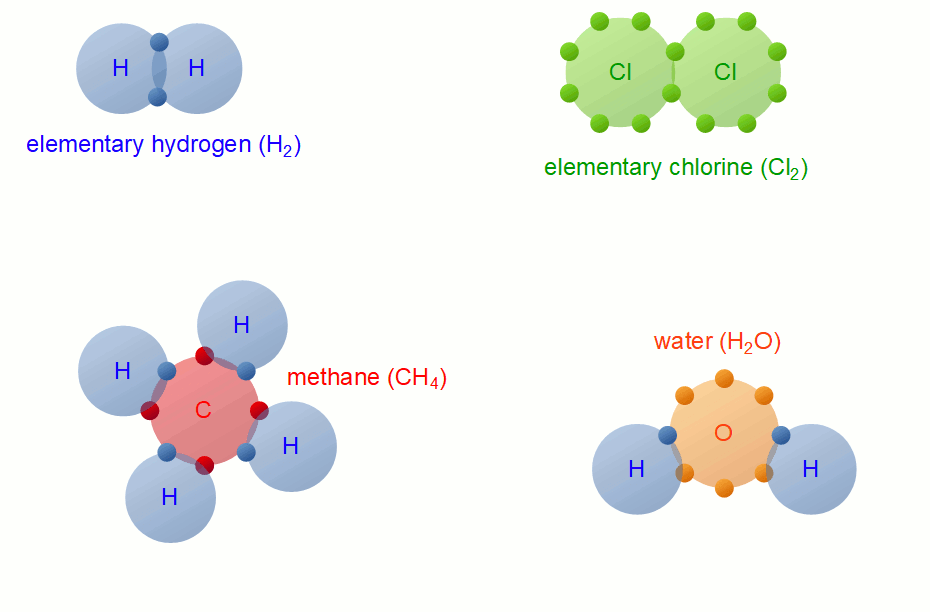
Ikatan kovalen tunggal adalah ikatan kovalen yang mana masing-masing atom menyumbang satu elektron untuk digunakan bersama dalam berikatan. Contoh ikatan kovalen tunggal yaitu: H2, HCl, H2O, Cl2, PCl3, PCl5, NH3, CH4, HF, CCl4. 1. Ikatan Kovalen Tunggal H2 2. Ikatan Kovalen Tunggal HCl 3. Ikatan Kovalen Tunggal H2O 4. Ikatan Kovalen Tunggal Cl2 5.

3 contoh senyawa ion kovalen dan logam Alexandra Springer
Adapun contoh ikatan kovalen rangkap tiga adalah C 2 N 2 , CO, dan N 2. Agar lebih jelas, yuk simak pembahasan berikut mengenai ikatan kovalen rangkap tiga.. Senyawa CH 4 atau metana juga termasuk salah satu ikatan kovalen non polar. Senyawa ini memiliki bentuk yang simetris, artinya tidak ada pasangan elektron bebas pada struktur molekul.

Ikatan Kovalen
Adapun untuk contoh senyawa dengan ikatan kovalen rangkap tiga yaitu C 2 H 2, HCN, dan lain lain. Ikatan kovalen koordinasi; Jenis lain dari ikatan kovalen adalah ikatan kovalen koordinasi. Pada dasarnya ikatan kovalen koordinasi sama seperti pada ikatan kovalen yang lain yaitu melibatkan penggunaan bersama pasangan elektron.

Detail Contoh Senyawa Ikatan Kovalen Koleksi Nomer 7
Jelaskan pengertian ikatan kovalen! Jawaban: Ikatan kovalen adalah ikatan yang terjadi karena pemakaian bersama pasangan elektron oleh dua atom yang berikatan. Soal No. 12. Sebutkan sifat-sifat umum senyawa kovalen! Jawaban: Terbentuk dari atom non logam dengan atom non logam; Pada suhu kamar berwujud gas, sebagian ada yang berwujud cair dan padat

Ikatan Kovalen Koordinasi, Kenali Pengertian dan Contohnya
Contoh ikatan kovalen koordinasi. 1. Senyawa SO3. Atom 16S memiliki konfigurasi elektron 2 8 6. Jadi, atom ini memiliki enam elektron valensi. Atom 8O memiliki konfigurasi elektron 2 6. Untuk membentuk senyawa SO3 yang memenuhi kaidah oktet, sepasang elektron dari atom S akan berikatan dengan sepasang elektron dari atom O sehingga membentuk.
125 Contoh Senyawa Kovalen dalam Kehidupan Seharihari Materi Kimia
Dilansir dari Chemistry Learner, ikatan kovalen tunggal adalah jenis ikatan kimia di mana atom-atom dalam suatu senyawa berbagi sepasang elektron. Artinya, atom yang berikatan secara kovalen tunggal hanya menggunakan dua elektron secara bersamaan (satu pasangan elektron sama dengan dua atom). Baca juga: Jenis-Jenis Ikatan Kimia. Contoh senyawa.

Ikatan Kovalen H2So4
Senyawa kovalen adalah senyawa kimia yang terbentuk karena adanya ikatan kovalen. Dalam kehidupan sehari-hari, banyak sekali contoh senyawa kovalen yang dapat kita jumpai. Diantara senyawa-senyawa kovalen tersebut adalah sebagai berikut.
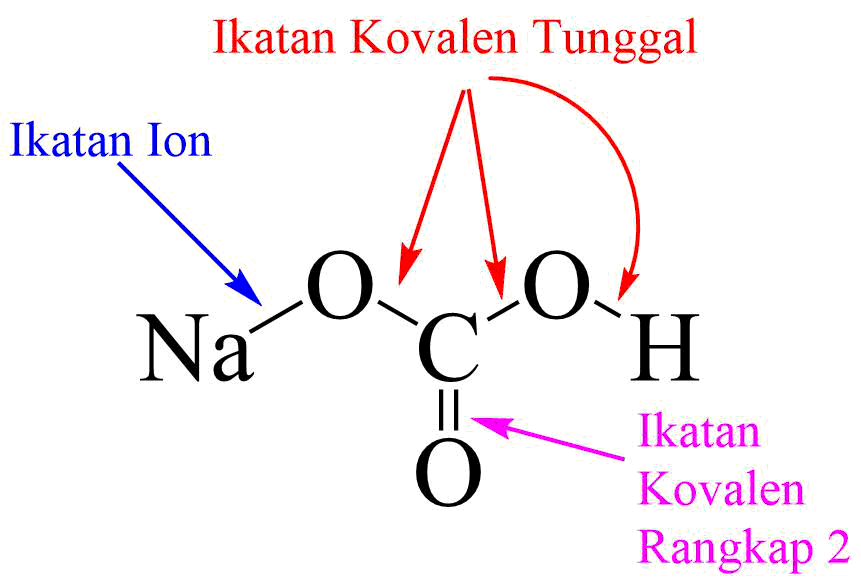
19 Contoh Senyawa yang Mempunyai Ikatan Ion dan Kovalen Sekaligus Materi Kimia
Senyawa kovalen non polar juga biasanya memiliki bentuk gas atau cair pada suhu kamar. Baca juga: Ikatan Kovalen Koordinasi: Pengertian dan Contohnya. Ikatan kovalen non polar terjadi karena kesamaan keelektronegativan atom-atom yang saling terikat. Di mana jika perbedaan keelektronegativan dua atom di bawah 0,4.
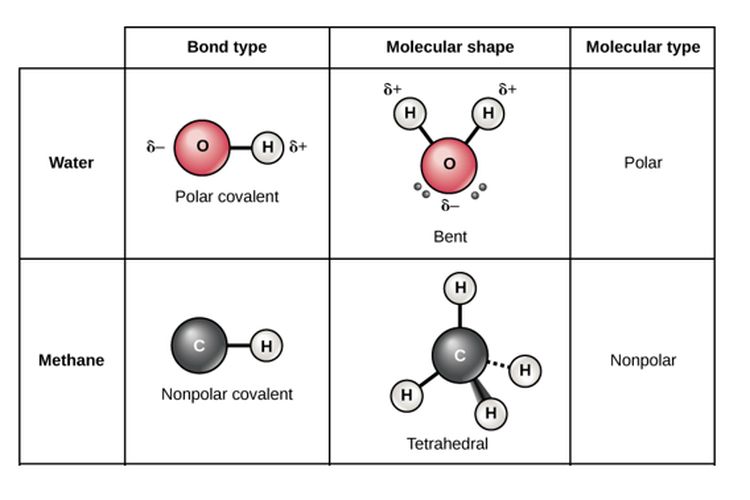
Foto Senyawa yang Mempunyai Ikatan Kovalen Tunggal
Contoh ikatan kovalen polar: HF. Contoh ikatan kovalen polar HF. Dlm senyawa HF ini, F mempunyai keelektronegatifan yang tinggi jika dibandingkan H.. sehingga pasangan elektron lebih tertarik kearah F, akibatnya akan terbentuk dipol-dipol atau terjadi pengkutuban (terbentuknya kutub antara H dan F). 2. Ikatan Kovalen Nonpolar